“过程”为研究RNA提供新方法,川大团队揭示四膜虫核酶自剪接动力学背后机制
今天,很高兴为大家分享来自DeepTech深科技的为研究RNA提供新方法,川大团队揭示四膜虫核酶自剪接动力学背后机制,如果您对为研究RNA提供新方法,川大团队揭示四膜虫核酶自剪接动力学背后机制感兴趣,请往下看。
来源:DeepTech深科技
四膜虫由于可在实验室里培养,因此从早年开始,它即是一种实验生物学上所使用的模式生物,并作为范例与工具研究各种基础生物学的现象。1982 年,美国科学家汤姆·切赫(Tom Cech)发现在嗜热四膜虫中,可以通过两步转酯反应完成自我剪接过程的 I 类自剪接内含子,事实上这是一种在没有蛋白参与前提下就能拥有酶催化活性的 RNA。并将其称为“核酶”。
2021 年,来自四川大学华西医院生物治疗国家重点实验室苏昭铭研究员团队在 Nature 上发表了论文。他们第一次对全长四膜虫核酶的 3.1Å 冷冻电镜结构进行解析,并展示了核酶结合底物前后的构象变化。
I 类自剪接内含子像其他 RNA 和 RNA- 蛋白质复合物一样,在完成两个酯交换反应时,会发生多次构象变化,裂解内含子并连接外显子。但是,这一动态过程的原子级模型仍不清楚,这限制了对 RNA 催化过程的动力学和分子机制的理解。

2023 年,该团队利用自制的四膜虫内含子,以 2.84–3.73Å 的分辨率获取了与自剪接过程相关的多种构象结构,相对完整地阐述了四膜虫核酶自剪接动力学过程的机制。
该研究为核酶催化机制提供必要的结构信息并推动了核酶研究进展。同时,补充了目前有限的 RNA 分子结构数据库,丰富了对 RNA 分子催化、折叠机理的认知。此外,该研究还进一步证明了 cryo-EM 在研究 RNA 动力学构象变化过程的潜力。
他们让转录共折叠后的四膜虫内含子直接进行自剪接反应,并使用冷冻电镜揭示了与自剪接相关的 6 种构象,分辨率在 2.84-3.73Å。其中,第一步反应包含了 P1 对接过程中的的 3 种构象;第二步反应的三种构象中,有一种状态携带由 5'- 外显子、5'- 内含子和 3'- 外显子共同形成的不可预见的假结结构。
该团队提供了外显子调节 I 类内含子 C1 亚型之间保守的剪接活性的例子。核苷酸易位可以在螺旋对接和内含子剪接中观察到,而金属离子的识别验证了普适的双金属离子剪接机制。
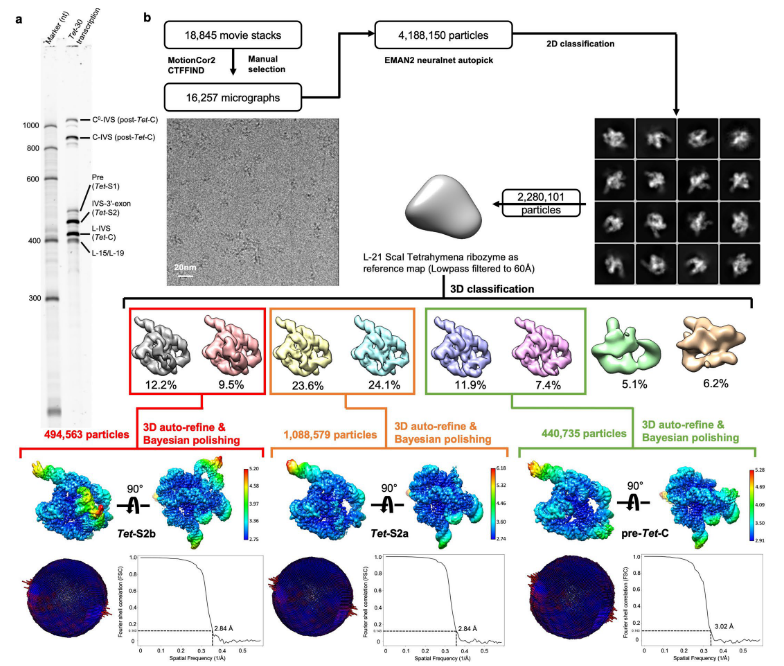 图丨四膜虫内含子自转录自剪接的低温电镜工作流程(来源:Nature Catalysis)
图丨四膜虫内含子自转录自剪接的低温电镜工作流程(来源:Nature Catalysis)在第一次反应之前,研究人员观察到两个与未对接的 P1 在初始态和中间态的动态构象,显示了一个可信的 P1 对接路线。对接后,J1/2 发生构象变化,使 P1-P2-P2.1 界面稳定,并与 J4/5 和 J8/7 一起确保 P1 对接和第一步剪接的准确性。
正在进行的剪接反应允许观察活性部位的天然金属离子环境,并为发生在剪接第二步的双金属离子机制提供证据。这些结果为四膜虫内含子自剪接的动态过程提供了一个具有结构和机制的全局图像,并证明了冷冻电镜在 RNA 介导的动态过程研究中的潜力。
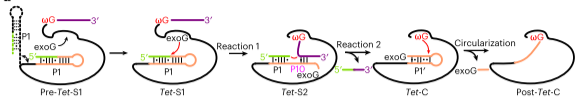
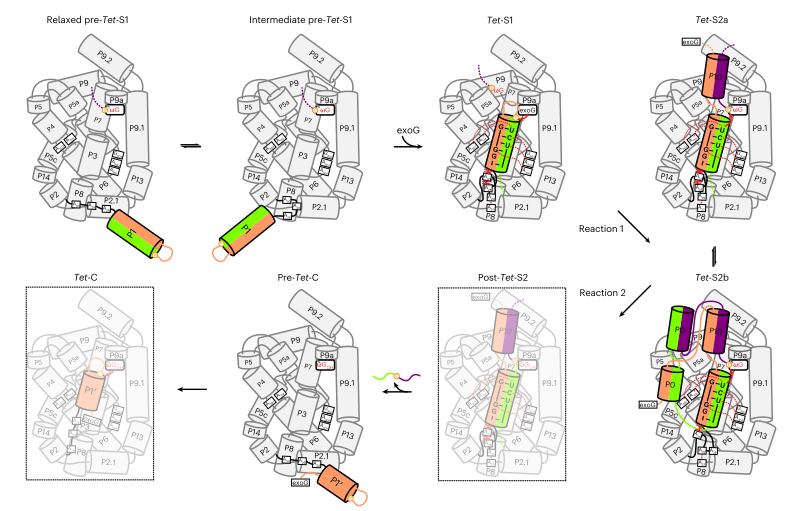 图丨四膜虫 I 类内含子自剪接过程示意图(来源:Nature Catalysis)
图丨四膜虫 I 类内含子自剪接过程示意图(来源:Nature Catalysis)据苏昭铭介绍,相较于传统的晶体学,冷冻电镜可以捕捉反应过程中更多不同的状态,这样就有利于研究人员更好地去观察研究。同时,据苏昭铭介绍,研究过程中遇到了一些挑战。
首先,如何设计外显子,不同长度的外显子会影响研究人员的观察内容。其次,在研究中,是需要在一个持续的反应过程中选择一个合适的时间点去观察,整个反应最核心的还是第一步。因此,需要精心设计反应条件和加入不同的底物去使第一步反应更容易被捕捉。
最后,解析出来新的外显子它们的分辨率不高,通过合作者基于中等分辨率电镜密度图的 RNA 建模算法,将 RNA 模型搭进密度图中。
苏昭铭表示,冷冻电镜技术在两方面展现出应用潜力。第一,该技术可以为将来研究 RNA 或者 RNA 蛋白复合物的动态过程结构提供新的方法。第二,通过解析发现了小分子结合点,可以基于此设计一些靶向 RNA 的小分子,从而为靶向 RNA 的小分子药物提供了可能。
随着人工智能的快速发展,目前人工智能已为很多学科提供了较为明显的帮助。为此,苏昭铭谈到了人工智能在预测蛋白质结构上的一些看法。
他认为,现有的预测蛋白质三维结构的一些算法在直接运用到 RNA 三维结构预测时都还有很大的难度和挑战,结果准确度低。如果将冷冻电镜观测和人工智能算法结合,将会为揭示一些动态过程以及折叠结构的预测提供更精确的结果。
参考资料:
1.Luo B, Zhang C, Ling X, et al. Cryo-EM reveals dynamics of Tetrahymena group I intron self-splicing. Nature Catalysis 6, 298–309 (2023). https://doi.org/10.1038/s41929-023-00934-3
运营/排版:何晨龙
好了,关于为研究RNA提供新方法,川大团队揭示四膜虫核酶自剪接动力学背后机制就讲到这。
版权及免责声明:凡本网所属版权作品,转载时须获得授权并注明来源“科技金融网”,违者本网将保留追究其相关法律责任的权力。凡转载文章,不代表本网观点和立场,如有侵权,请联系我们删除。
相关文章
- “考生”下半年自考即将开始 省考试院发出温馨提示
- “父亲”父亲的眼神杀
- “这是”自内耗到自洽
- “大桥”G3铜陵长江公铁大桥先导索过江
- “某甲”父亲被羁押继母要离婚,未成年女儿谁来抚养?法官多方努力,难题解决了!
- “亚马逊”哪些以色列芯片公司已被美国企业收购?
- “结构”结核杆菌致病机制获揭示
- “装修”装修公司老板明知公司亏损仍吸引客户签合同,骗取上百人700余万,被判11年
- “射电”穿越80亿光年的快速射电暴源于一场“星系交通事故”
- “必胜客”必胜客最黑暗的料理来了
- “结构”结核杆菌致病机制获揭示
- “湍流”流向旋转槽道中的多尺度动力学研究新进展
- “口信”支持外贸稳规模优结构,金融监管总局发文加强出口信保公司地市级分支结构管理
- “原位”康奈尔团队发展原位成像技术,揭示锂硫零级反应动力学及转化机制
- “无图”极越CEO夏一平:无图智驾是逐步迭代的过程,无法一蹴而就
- “北京大学”一个漫长痛苦的过程!他们终获“学科交叉的胜利”
- “结构性”终于松口了!
- “乙炔”新过程用水直接加氢乙炔制乙烯
- “核糖核酸”我国科学家揭示外源核酸诱导的原核生物短Ago蛋白系统发挥功能的分子机理
- “核糖核酸”原核短Ago系统在病毒入侵前后有啥变化?研究揭示









