“疫苗”继往开来,展望诺奖后mRNA药物的未来
今天,很高兴为大家分享来自DeepTech深科技的继往开来,展望诺奖后mRNA药物的未来,如果您对继往开来,展望诺奖后mRNA药物的未来感兴趣,请往下看。
来源:DeepTech深科技
本文作者 2:美国麻省理工学院戴维·H·科赫癌症综合研究所(David H. Koch Institute for Integrative Cancer Research)博士后研究员胡一宗博士

图丨本文作者:美国约翰霍普金斯大学纳米生物技术研究所博士研究生李思轩(左),美国麻省理工学院戴维·H·科赫癌症综合研究所(David H. Koch Institute for Integrative Cancer Research)博士后研究员胡一宗博士(来源:资料图)
2023 年诺贝尔生理学或医学奖于本周一揭晓,授予匈牙利生物化学家卡塔琳·卡里科(Katalin Karikó)和美国医学家德鲁·韦斯曼(Drew Weissman),以表彰他们在 mRNA 核苷碱基修饰方面的发现,使新冠 mRNA 疫苗的开发成为可能。
在 mRNA 疫苗出现之前,现代疫苗通常由灭活病毒或病毒片段(蛋白质或者多糖等等)组成,通过免疫系统的识别和激活让人体产生免疫反应,如乙型肝炎病毒疫苗和人类乳头瘤病毒疫苗。实际生产中,基于病毒或蛋白质的疫苗需要在活细胞中生产。
整个工艺不仅耗时,而且需要在制造中严格控制纯化、储存、运输过程以保证蛋白质的结构和活性。早在上世纪七十年代,生物学家们就开始探索蛋白质疫苗另外的可能性:将编码病毒蛋白的 mRNA 递送到细胞中,并诱导细胞将 mRNA 翻译为蛋白质[1]。这项技术如果成功,意味着可以大大缩短疫苗平台的研发和生产周期并实现大规模生产,将具有开创性意义。
 第一块拼图:mRNA 碱基修饰
第一块拼图:mRNA 碱基修饰然而,mRNA 作为疫苗的安全性是首要解决的问题。未经修饰的合成 mRNA 具有免疫原性——向人体递送外源性 RNA 会引起自身防御机制。
即使有 mRNA 逃过循环系统中 RNA 酶的分解进入细胞,也会触发一系列来自细胞的固有免疫防御,阻止 mRNA 的表达。卡里科和韦斯曼在合作开发针对艾滋病的 mRNA 疫苗过程中,也观察到了 mRNA 在注射到小鼠体内后产生了强烈的非特异性免疫反应。针对这一现象,他们发现合成的 mRNA 激活了一连串名为 Toll 样受体(TCR)的免疫传感器,这些受体能在第一时间对来自病原体的危险信号作出响应[2]。
2005 年,两人指出,通过重新编排 mRNA 的一个核苷酸(尿苷)的化学键,合成一种名为假尿苷的类似物能使 mRNA 不再被免疫系统识别,由此带来的效力提升体现为非特异性免疫反应的降低和近三个数量级的蛋白质表达的提升[3]。这一发现为日后的 RNA 作为疫苗的临床应用奠定了基础。
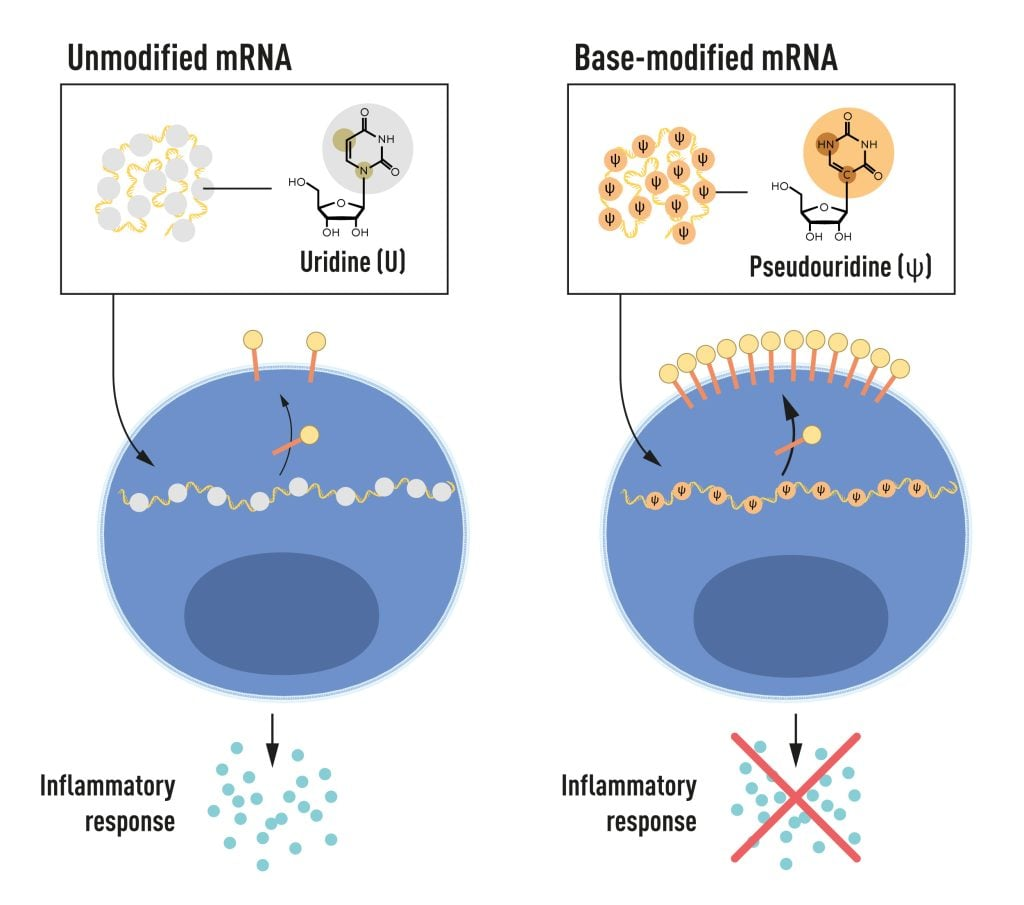 图|
图|卡里科和韦斯曼发现将碱基修饰过的 mRNA(用假尿苷 ψ 替换尿苷 U)递送到细胞中可以阻止细胞产生炎症反应并增加蛋白产量(来源:诺贝尔奖官网)
 第二块拼图:mRNA 递送系统
第二块拼图:mRNA 递送系统mRNA 疗法的第二个突破来自 RNA 递送技术。体外合成的 mRNA 自身并不稳定,将 mRNA 转运到动物细胞内这一过程需要额外的保护,以避免受到环境中的 RNA 酶的和细胞中溶酶体逃逸前的水解。另外 mRNA 本身高度负电及其生物大分子的属性使得其难以凭借自身跨越细胞膜,不能直接被细胞摄取。来自加拿大不列颠哥伦比亚大学的生物化学家 Pieter Cullis 使用脂质纳米颗粒(lipid nanoparticle, LNP)作为载体实现 RNA 的封装和递送[4]。
脂质纳米颗粒含有四种脂质组分:可电离的阳离子脂质、磷脂、胆固醇和聚乙二醇(PEG)修饰的脂质。四个组分共同决定纳米颗粒结构和稳定性、递送转染效率、和安全性。可电离的阳离子脂质在酸性 pH 值条件下带正电,通过与带负电的 mRNA 结合,与其他组分自组装形成 LNP。可电离阳离子脂质的酸解离常数(pKa)使得其能在生理条件下(如在血液中)使 LNP 的表面电荷变成中性或弱负电性,在减小细胞毒性的同时,增加其体内存留时间。当进入内吞体后,其重新质子化引起和内吞膜的强烈相互作用,破坏内吞膜的同时有效地将核酸释放到细胞质中。
自此两块拼图完整嵌合,mRNA-LNP 技术平台的可行性走通,实现了对 mRNA 的有效递送。面对新冠爆发,依靠 mRNA 疫苗的优势, Moderna 在 10 周内与美国国家过敏和传染病研究所(NIAID)合作完成小鼠研究和人体试验;BioNTech 与制药公司辉瑞(Pfizer)合作,在不到 8 个月的时间里完成从首次人体试验到紧急使用批准的流程;2020 年 8 月,辉瑞和 BioNTech 联合研制的疫苗 BNT162b2 成为第一个获得 FDA 全面批准的 mRNA 疫苗。

图|包封 mRNA 的脂质纳米颗粒(LNP)。四组分分别为可电离的阳离子脂质(DLin-MC3-DMA 为 Onpattro 配方;SM-102 为莫得纳配方;ALC-0315 为辉瑞和 BioNTech 配方)、胆固醇、磷脂、和聚乙二醇(PEG)修饰的脂质(来源:Nature Reviews Drug Discovery[5])

机遇与挑战:新冠疫苗以外的 mRNA 药物
mRNA 疫苗的免疫机理同时可以应用于癌症,通过使 mRNA 序列表达肿瘤相关抗原、肿瘤特异性抗原、甚至病人肿瘤中的个性化抗原,在肿瘤外环境中对免疫系统的刺激即能训练和激活免疫细胞识别这些抗原,杀伤癌细胞。
2022 年 12 月,莫德纳(Moderna)的一款候选肿瘤疫苗药物(代号 mRNA-4157)联合默沙东 PD-1 单抗的疗法在针对黑素瘤的二期临床实验中取得了降低复发率和死亡率的预期效果;2023 年 5 月,BioN Tech 在《自然》期刊发表论文,汇报其候选肿瘤疫苗(代号 BNT-122)联合化疗疗法在针对胰腺导管腺癌的一期临床实验中取得了降低手术后复发率的预期效果[6]。
这些积极的结果标志着癌症疫苗概念验证的初步成功,即由 mRNA 疫苗引起的免疫反应足以引起实质性的肿瘤细胞杀伤,并部分克服了肿瘤内的免疫抑制环境,或许预示着癌症治疗新时代的黎明已经到来。
除肿瘤外,mRNA 药物还可以通过表达各种蛋白可以实现过表达、激活、抑制和删除目的基因等目的,作为药物治疗包括心血管以及神经系统疾病、自身免疫性疾病、遗传性疾病等在内的多种疾病。在 mRNA 疗法带来广泛的应用前景的同时,挑战与机遇并存。
mRNA 疫苗发挥效力只需要生产少量蛋白即可诱导免疫,而 mRNA 疗法提出了更多的要求,包括对蛋白表达量的精确调控,同时减小 mRNA-LNP 可能引起的免疫过度和炎症等不良反应。目前我们认为 mRNA-LNP 平台还存在着若干亟待解决和优化的问题:靶向递送的效率问题,生产储存运输质控问题,对递送载体的组装机理及表征的问题,通过工程方法进一步提高递送效率的问题。
靶向性问题:实现靶向递送 mRNA 药物需要建立在对其递送机理的深入理解的基础上。目前 mRNA 药物在体内的递送过程以及生物相互作用复杂,涉及淋巴及血液循环、组织间质转运、与细胞结合、胞内转运等过程,很多机理目前尚未阐明。在循环过程中,LNP 会吸附血液、组织液中内源性大分子形成“蛋白冠”。
研究者发现载脂蛋白 E(ApoE)吸附是介导脂质纳米粒肝脏靶向的重要原因[7]。用作 mRNA 疫苗的 LNP 递送系统的配方目前均为肝脏靶向主导。而肝外靶向到特定的器官或组织,包括大脑、骨髓、肺部、脾脏等等器官,是目前的研究热点。通过改变 LNP 配方四个脂质的组分,或添加额外的辅助脂质,可以实现对“蛋白冠”组分的调控以实现将 LNP 递送到肺、脾脏和肝脏[8]。
主动靶向递送策略通过在 LNP 表面添加多肽、抗体及抗体片段、核酸适配体等等靶向分子,实现 LNP 与组织或细胞的受体特异性识别和结合,从而增加 mRNA 对特定组织或细胞的有效递送,降低毒性。总之,对靶向性问题的研究有助于揭示纳米药物体内过程,有助于理清 mRNA-LNP 在免疫、炎症等关键生理过程中的作用,推动更多临床转化和精准用药。

图|集成式模型解释脂质纳米颗粒(LNP)介导的小干扰 RNA(siRNA)体内递送到肝细胞。关键步骤包括聚乙二醇脂质从 LNP 表面脱落同时内源载脂蛋白 E(ApoE)被募集到 LNP 表面,LNP 被转运跨过帘式内皮膜并与低密度脂蛋白受体(LDLR)结合,被胞吞并实现内涵体逃逸从而释放 siRNA 进入细胞质发挥功能(来源:Nature Nanotechnology[4])
对递送载体的组装机理及表征的问题:深刻理解 LNP 结构和功能之间的关系,也是推动核酸疗法这一先进的技术向前发展的关键。进一步研究 RNA-LNP 的结构和组成对于配制及生产稳定有效的纳米颗粒具有关键意义。
作为 mRNA 药物载体的 LNP 配方的复杂性(四组分性质及其配比)决定了多个关键参数都可以被同时影响,可谓牵一发而动全身。LNP 的理化特性,包括尺寸、表面电荷(Zeta 电位)和表面修饰,对 LNP 的功效、药代动力学和生物分布有直接影响。比如 LNP 尺寸对整体药物的靶向性,循环寿命以及转染效率有直接影响;表面电荷影响 LNP 的循环清除。因此负载核酸的包封效率,粒径等关键质量属性(Critical Quality Attributes,CQAs)均被要求在生产制造中披露。
而其他影响 LNP 结构和功能关键参数的表征如核酸载荷量,空包率等[9]尚未纳入 FDA,药典。我们预计今后会有更多全面深入的分析表征技术涌现,以完善对 LNP 制剂生产关键因素的认识。
通过工程化方法进一步提高递送效率的问题:LNP 递送体系的核心是可电离脂质,也是专利争夺的核心。已有的研究表明特定的脂质结构,比如支化结构、特定的疏水尾部长度、以及非饱和官能团,可以提高 mRNA 细胞内递送的效率。
基于这些合理设计(Rational design)进行的研究产出了多个正在应用于临床的候选脂质结构。但在更多情形下,很多意想不到的结构却能带来很好的效果。为了能快速筛选出这样的结构,全球各地的研究者采用多种简洁、组合性质的合成路径构建大规模化学结构文库。
有些文库的构建实现了自动化生产,并在粗产物就有很高的产率,使得不进行纯化就在体外细胞中进行大规模实验成为了可能。这种文库方法筛选出了大量高效的可电离化脂质,同时也产出了大量的结构-功能对应数据。随着近年来人工智能技术的发展,这些规模庞大的数据被用来训练人工智能模型,这些模型被用来预测科学家一般很难直接设计,或完全存在于化学结构文库以外的结构。
从已经探索的化学结构的规模来看,目前已被研究成功设计和合成的结构可能还仅仅是所有有效结构的很小一部分;从结果上来看,这些进展或多或少地提高了 mRNA 递送的效率,但都没有形成质的的飞跃,即极大地提高 LNP 逃逸内吞体的能力,或极大地提高靶向递送的能力。除可电离脂质外,化学修饰 LNP 其他组分的结构也是活跃的研究领域。
对科学研究的启示:卡里科和韦斯曼获奖是颇为科学界和大众所称道的。在 mRNA 药物的雏形期,这一技术曾被同时代的专家形容得一文不值[10]。诚然,mRNA 药物的成功是颇具理想主义色彩的故事,是个人的努力同环境阻力抗争的成功,是三十年磨一剑坚持的结果。
在众多新闻报道和公众号推送中, “冷板凳”一词被频频提及,宾夕法尼亚大学在这一技术问世和成功前的态度也为众人讨论。这些故事对于我们这样的青年学者来说是很有冲击力的。如果把我们置于像卡里科和韦斯曼当时的情形下,能否坚持自己所相信的研究?在全球科学研究投入规模呈指数级增长,年学术发表较世纪初提升近三倍的今天,我们的科学研究环境是否让像卡里科和韦斯曼这样的人能遇到更少阻力呢?这些故事背后的另一面也值得我们每个人深思。
参考文献:
1.X. Hou, T. Zaks, R. Langer, and Y. Dong, “Lipid nanoparticles for mRNA delivery,” Nat. Rev. Mater., vol. 6, no. 12, pp. 1078–1094, 2021.
2.K. Karikó, H. Ni, J. Capodici, M. Lamphier, and D. Weissman, “mRNA Is an Endogenous Ligand for Toll-like Receptor 3,” J. Biol. Chem., vol. 279, no. 13, pp. 12542–12550, 2004.
3. K. Karikó, M. Buckstein, H. Ni, and D. Weissman, “Suppression of RNA recognition by Toll-like receptors: The impact of nucleoside modification and the evolutionary origin of RNA,” Immunity, vol. 23, no. 2, pp. 165–175, 2005.
4.A. Akinc et al., “The Onpattro story and the clinical translation of nanomedicines containing nucleic acid-based drugs,” Nat. Nanotechnol., vol. 14, no. 12, pp. 1084–1087, 2019.
5. N. Chaudhary, D. Weissman, and K. A. Whitehead, “mRNA vaccines for infectious diseases: principles, delivery and clinical translation,” Nat. Rev. Drug Discov., vol. 20, no. 11, pp. 817–838, 2021.
6.L. A. Rojas et al., “Personalized RNA neoantigen vaccines stimulate T cells in pancreatic cancer,” Nature, vol. 618, no. 7963, pp. 144–150, 2023.
7.A. Akinc et al., “Targeted delivery of RNAi therapeutics with endogenous and exogenous ligand-based mechanisms,” Mol. Ther., vol. 18, no. 7, pp. 1357–1364, 2010.
8.S. Liu et al., “Membrane-destabilizing ionizable phospholipids for organ-selective mRNA delivery and CRISPR–Cas gene editing,” Nat. Mater., vol. 20, no. 5, pp. 701–710, 2021.
9.S. Li et al., “Payload distribution and capacity of mRNA lipid nanoparticles,” Nat. Commun., vol. 13, no. 1, p. 5561, 2022.
10.E. Dolgin, “The tangled history of mRNA vaccines,” Nature, vol. 597, no. 7876, pp. 318–324, 2021.
运营/排版:何晨龙

好了,关于继往开来,展望诺奖后mRNA药物的未来就讲到这。
版权及免责声明:凡本网所属版权作品,转载时须获得授权并注明来源“科技金融网”,违者本网将保留追究其相关法律责任的权力。凡转载文章,不代表本网观点和立场,如有侵权,请联系我们删除。
相关文章
- “小行星”我国2030年前后 实现载人登月
- “都是”A股的觉醒之年!
- “孩子”一生的功课
- “益康”倍益康上市几个月收入净利都大减 市值仅几亿 创始人张文有啥办法?
- “科幻”嘉宾共话科幻的未来:被视为“珍贵市场”,中国科幻正青春
- “灯会”红星观察|自贡灯会走出“春节舒适区”:首次试水中秋国庆主题灯会火出圈背后
- “华为”新麒麟全面替代!曝华为正在清理骁龙机型库存:掀起全线新品的“洪流”
- “鸟类”评论丨大楼玻璃贴膜防鸟撞,城市的天空如何助鸟自由飞翔?
- “同济大学”四川“无臂青年”彭超参与杭州亚残运会火炬传递,曾用脚写字考上同济大学研究生
- “模型”人工智能公司OpenCSG发布大模型开源生态社区“传神”
- “疫苗”最高补贴600元!成都适龄女生九价HPV疫苗首针开打
- “疫苗”百克生物被“卷”带状疱疹疫苗 江湖纷扰又多不确定
- “疫苗”HPV疫苗之后再揽200亿订单,智飞生物又抱到了新「大腿」|焦点分析
- “疫苗”疫苗龙头艾美疫苗上市一周年:重启回A计划后股价腰斩,累计亏损超10亿元
- “疫苗”涨停!手握HPV疫苗的智飞生物,又拿下GSK带状疱疹疫苗独家代理权
- “疫苗”张文宏:mRNA疫苗技术落地是人类文明史上的又一次“盗火”
- “疫苗”诺奖得主加盟的BioNTech,创始人夫妇是如何打造这家全球生物科技巨头的?
- “靶向”研究揭示调控肿瘤耐药和转移的新机制
- “疫苗”世卫组织批准第二种儿童疟疾疫苗
- “疫苗”科普:为mRNA疫苗快速研发奠定基础——2023年诺贝尔生理学或医学奖成果解读









