“这一”哈佛团队拓展GPS-peptidome技术,成功发现16组E3-降解子对
今天,很高兴为大家分享来自DeepTech深科技的哈佛团队拓展GPS-peptidome技术,成功发现16组E3-降解子对,如果您对哈佛团队拓展GPS-peptidome技术,成功发现16组E3-降解子对感兴趣,请往下看。
来源:DeepTech深科技
细胞信号传导是一个复杂的通讯网络,由功能分子机制之间的交互构成。这种通讯协调着细胞内事件,使细胞能够感知环境条件并作出适当的反应。
细胞信号传导机制中的一个主要方式:是通过蛋白质降解来实现调控。通过在响应不同的环境条件时有针对性地降解蛋白质,细胞可以迅速调节特定蛋白质的活性,从而调控下游细胞信号传导。
选择性降解,主要由泛素-蛋白酶体系统来调节。其中,大约有 600 种 E3 泛素连接酶负责降解约 20000 种蛋白质。
深入了解这一复杂的选择性蛋白质降解网络,对于理解细胞信号传导至关重要。
在泛素-蛋白酶体系统中,一个重要的问题是如何实现底物的识别特异性。换句话说,这个问题的核心在于从机制上来说,600 种 E3 泛素连接酶如何识别约 20000 种蛋白质作为它们的底物?
20 世纪 80 年代,一支国外团队的研究表明 E3 通过识别短线性肽段,即所谓的降解子来识别底物(尽管这不是唯一的识别机制)。
此后,大量文献证实降解子的识别,是 E3 泛素连接酶常用的一种识别机制。然而,已知的降解子数量仍然有限,部分原因是由于缺乏用于降解子鉴定的高通量技术。
2018 年,哈佛大学教授斯蒂芬·埃利奇(Stephen J. Elledge)实验室开发了 GPS-peptidome 技术。这是一种高通量系统,结合了肽体筛选来识别降解子肽段,并结合 CRISPR 筛选将降解子肽段与它们对应的 E3 连接酶进行配对。
2018-2019 年,埃利奇课题组利用 GPS-peptidome 技术来研究 C 端降解子[1]和 N 端降解子[2]。然而,大多数降解子是“内部”的,而这一大类降解子长期以来一直未被系统化研究。因此,该团队决定利用 GPS-肽体组技术来研究这些内部降解子。
与 N/C 端降解子不同,内部降解子的识别与位置无关。所以,需要更长的模体来实现识别特异性。
这一特性带来的影响是:利用终端降解子相关论文中介绍的方法,很难去识别内部降解子性。
为克服这一难题,埃利奇课题组专门开发一个用于分析内部降解子的流程,结合了机器学习、高通量突变实验、以及自研的基于突变特征的降解子聚类算法。
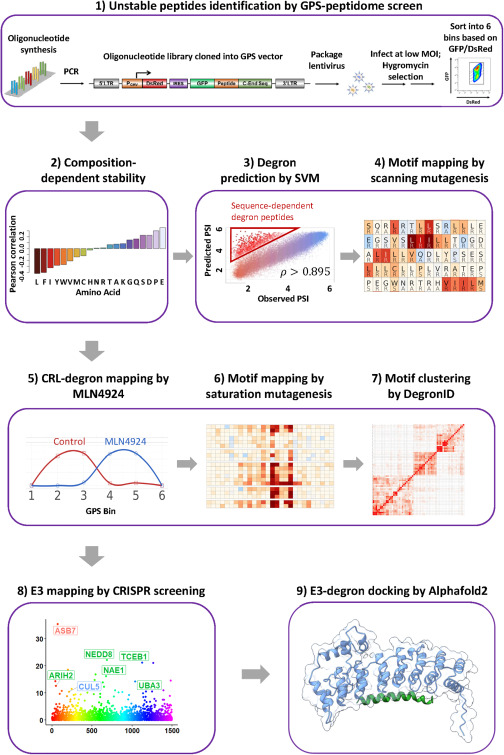 (来源:Molecular Cell)
(来源:Molecular Cell)未来,假如将这个框架扩展成更大规模的资源类项目,人们或能针对降解子景观实现系统级理解。
据介绍,本次项目始于 2020 年底。由于涉及大量的实验工作和技术细节需要克服,因此在 2021 年,课题组开展大量实验来验证最初的设想,即结合 GPS-peptidome 技术、机器学习和实验方法,寻找更多的内部降解子以及它们对应的 E3 连接酶。
在研究过程中,他们还研发了 DegronID 算法,这是一种基于突变特征对降解子肽段进行分类的算法。在获得大规模突变特征后,导师埃利奇意识到可以设计一个客观且高效的算法来进行分类,并邀请本次论文的共同第一作者布兰登·希(Brandon Sie)来开发这一算法。
张之谦表示:“这个想法取得了巨大成功,也成为论文的一个关键成果。2022 年底,当我们确认已经找到 16 组 E3-降解子对后,我们认为论文的核心概念已经初步形成,于是着手撰写论文并提交投稿。”
他继续说道:“事实上当我开始这个课题时,已经是我的博士第四年,这个课题非常庞大,不太容易由一个博士生独自掌握,同时也伴随着一定风险。”
然而,导师给予了他充分的支持,并没有因为张之谦前两年的“失败”经历而计较,同时提供了许多深刻见解和建议。
“经过六年的博士研究,我深刻认识到导师的科研水平和指导对一个学生学术发展的关键作用。在 20 世纪 90 年代,我的博士导师开创了 DNA 损伤信号领域,并因此获得了 Lasker Award 和 Breakthrough Prize 等一系列重要奖项。此后,他又在病毒学、免疫学、蛋白质降解、癌症等领域推动了许多高通量遗传技术的发展。能够在一个持续引领浪潮的实验室耳濡目染,对我的个人成长有很大的意义。”张之谦说。
在整个博士研究期间,张之谦深感做科研的不易。他总结称,如何区分坚持和固执,如何平衡战略和执行,如何兼顾理论和实践,是一个博士生的必修课。
多年下来,他自己也有了一些体会,却在毕业前发现这些思想早已被《孙子兵法》和《道德经》等先秦时期的诸子百家概括。
 图 | 张之谦(来源:张之谦)
图 | 张之谦(来源:张之谦)“这让我感受到中华传统文化的博大精深。若是能够在博士研究开始前接触这些思想,我在读博期间的收获或许会更大。”张之谦表示。
参考资料:
1. Koren, I., Timms, R. T., Kula, T., Xu, Q., Li, M. Z., & Elledge, S. J. (2018). The eukaryotic proteome is shaped by E3 ubiquitin ligases targeting C-terminal degrons. Cell, 173(7), 1622-1635.
2. Timms, R. T., Zhang, Z., Rhee, D. Y., Harper, J. W., Koren, I., & Elledge, S. J. (2019). A glycine-specific N-degron pathway mediates the quality control of protein N-myristoylation. Science, 365(6448), eaaw4912.
3. Zhang, Z., Sie, B., Chang, A., Leng, Y., Nardone, C., Timms, R. T., & Elledge, S. J. (2023). Elucidation of E3 ubiquitin ligase specificity through proteome-wide internal degron mapping. Molecular cell, 83(18), 3377-3392.
运营/排版:何晨龙
好了,关于哈佛团队拓展GPS-peptidome技术,成功发现16组E3-降解子对就讲到这。
版权及免责声明:凡本网所属版权作品,转载时须获得授权并注明来源“科技金融网”,违者本网将保留追究其相关法律责任的权力。凡转载文章,不代表本网观点和立场,如有侵权,请联系我们删除。
相关文章
- “这一”哈佛团队拓展GPS-peptidome技术,成功发现16组E3-降解子对
- “马斯克”马斯克又没管住嘴:或因网络发言损失5亿广告收益 穿防弹衣访问以色列欲控制损失?
- “中山”这一国家重大工程,通了!
- “消息”当苹果拥抱RCS,一石能否激起千层浪?
- “套餐”「健康焦虑」的年轻人,被高价体检拿捏
- “车主”零跑T03车主轻信他人刷机承诺 结果车机变砖损失5000
- “交通银行”交通银行与15家房企召开座谈会 拟进一步支持房企融资需求
- “要素”中央财大陈端:AI大模型将推动以数据资产为核心的产融协同创新
- “社区”国家卫健委:鼓励和支持社会力量建好婴幼儿家庭的“身边园”
- “院士”一个宿舍就三人,全当院士了
- “中山”这一国家重大工程,通了!
- “锅炉”代表世界最高水平!这一核心装备研制成功
- “长城”长城魏牌高管:绝不用增程 增程约等于三分之一混联
- “金牛”事关奖补及减税,这场培训提升技术合同登记规范性
- “细胞”为增殖细胞“装上GPS”:科学家打造单细胞追踪技术,成功解析小鼠大脑上万个新生细胞
- “中国移动”中国移动完成全球首个对称50G PON应用示范
- “马来”相机拍到濒危马来虎
- “京东”京东云技术升级 支持京东11.11成交额、订单量、用户数齐创新高
- “肾脏”改良抗真菌剂或增临床有效性安全性
- “英特尔”工业富联携手英特尔发布新一代先进散热技术